V dubnu minulého roku byla publikována zpráva z první fáze výzkumu vzácných onemocnění, který probíhá v CCP (Czech Centre for Phenogenomics). Jde o přehled výzkumných metod a nástrojů potencionálně použitelných k léčbě některých vzácných epigeneticky podmíněných nemocí.
Dokument je volně dostupný v celém rozsahu v původním textu v angličtině na tomto odkazu.
CO JE TO EPIGENETIKA?
Jedná se o vědní obor spadající pod genetiku, který zkoumá, jak mohou být určité znaky nebo vady ovlivněny aktivací či deaktivací určitých genů, aniž by byly následkem mutace DNA. Znaky nebo vady mohou být v některých případech předány z jedné generace na následující, aniž by byly součástí genetické informace v samotné DNA.
Označujeme tak jev, který mění expresi genů pomocí chemických modifikací DNA a chromatinu, aniž by změnil přímo genetický kód.
Zjednodušeně se dá pojem EPIGENETIKA vysvětlit tak, že si genom pamatuje určité vlivy prostředí, jimž byl vystaven.
Podstatou výzkumu je ovlivnění epigenomu. To je část genomu, jež má vliv na proces, díky kterému je v genu uložená informace převedena v existující buněčnou strukturu nebo funkci. Což má obrovský potenciál v případě řady vzácných onemocnění, u nichž jsou tyto geny nefunkční.
I když je před námi ještě mnoho výzev, systémy CRISPR nepochybně otevřely nové dveře pro léčbu vzácných imprintingových nemocí na základě editace epigenomu, což dříve nebylo možné.
Přehled nastínil možnosti dalšího vývoje výzkumu v oblasti léčby vzácných onemocnění pomocí nejnovějších metod molekulární biologie k ovlivnění exprese genů u Angelmanova syndromu a podobných nemocí jako Prader-Willi syndromu, Diabetes mellitus 1. typu a Silver-Russell syndromu.
VÝZKUM PŘEHLEDNĚ V NĚKOLIKA BODECH
NAVÁZÁNÍ SPOLUPRÁCE
V roce 2018 došlo k navázání spolupráce neziskové organizace ASGENT a CCP.
A hned následovalo určení, co se bude zkoumat – Definice výzkumného projektu. Cílem výzkumu je studium vybraných genů a biologických procesů, které se podílejí na vzniku Angelmanova syndromu. Jejich pochopení může být důležité pro nalezení léčby genetických vad.
ZAHÁJENÍ VÝZKUMU
Ještě ten samý rok provedlo CCP Review – souhrn problematiky v odborné literatuře a současné úrovně poznání, následoval – Návrh možných cest výzkumu a možných nových přístupů, ahned poté zahájení výzkumu.

V průběhu roku 2019 pak byly vytvořeny jedinečné zvířecí modely. Alfa a omega celého výzkumu.
ČÍM JSOU MYŠŠÍ MODELY JEDINEČNÉ?
První model – je jediněčný tím, že na rozdíl od jiných modelů ve světě, mu chybí nejen kódující, ale zároveň také nekódující části hlavního genu způsobujícího onemocnění. To tento model reálněji přibližuje skutečné situaci u pacientů.
Druhý model – chybí mu další, jiný gen spadající do postižené oblasti, který do této doby nebyl tímto způsobem v souvislosti s Angelmanovym syndromem zkoumán.
DALŠÍ KROK

Po úspěšném vytvoření několika jedinečných myších modelů vzácných onemocnění, vědci v roce 2020 pokračují zkoumáním fenotypových projevů Angelmanova syndromu na zvířecích modelech.To znamená, že zkoumají specifické vnější projevy, které porovnávají s kontrolní skupinou. Cílem bude podrobné popsání vlivu jednotlivých oblastí delece na vnější projevy (jako je např. hlasový projev, pohyb, aktivita v průběhu dne, energetický příjem a výdej, hmotnost, reflexy a další) a popsaní vlivu delecí na projevy jiných genů.

AKTUÁLNĚ
K našemu velkému potěšení výzkum od minulého roku pokročil zase dál a vědci mají rozpracované nové materiály, pokračují ve výzkumu a aktuálně pracují na možném terapeutickém postupu. Všichni se můžeme těšit na další pokroky, které nám dávají velkou naději.
Měli jsme možnost nahlédnout do aktuálně běžícího výzkumu, jeho výsledky ještě nejsou publikované, takže zatím můžeme říct jenom, že jde o další významný posun vpřed.
Podpora základního výzkumu dává smysl o to víc, že jeho výsledky jsou v mnoha případech uplatnitelné v léčbě mnoha jiných nemocí, nejen těch vzácných.
d
d
dd
d
Potenciál editace epigenomu pomocí CRISPR/Cas9 pro vzácná imprintingová onemocnění
Abstrakt:
Imprintingová onemocnění (IO) jsou vzácné vrozené poruchy způsobené aberancemi imprintovaných genů. Vzácné IO jsou tvořeny skupinou několika odlišných poruch, které sdílejí velkou míru homologie z hlediska genetické etiologie a příznaků. Narušení genetických nebo epigenetických mechanismů může způsobit problémy s regulací exprese imprintovaných genů, což vede k onemocnění. Genetické mutace ovlivňují imprintované geny, duplikace, delece a uniparentální disomie jsou opakující se jevy způsobující imprintingová onemocnění. Epigenetické změny metylačních značek v imprintingových kontrolních centrech rovněž mění expresní vzorce a většina pacientů se vzácnými ID nese intaktní, ale buď umlčené, nebo nadměrně exprimované imprintované geny. Kanonická editace CRISPR/Cas9 spoléhající se na opravu dvouřetězcových zlomů DNA má z hlediska terapie vzácných ID jen málo co nabídnout. Místo toho lze CRISPR/Cas9 využít sofistikovanějším způsobem, a to zacílením na epigenom. Katalyticky mrtvý Cas9 (dCas9) svázaný s efektorovými enzymy, jako jsou DNA de- a metyltransferázy a editory histonového kódu, vedle systémů, jako jsou CRISPRa a CRISPRi, prokázal vysokou účinnost editace epigenomu v eukaryotických buňkách. Tato nová éra editorů epigenomu CRISPR by pravděpodobně mohla změnit pravidla hry pro léčbu a ošetřování vzácných IO rafinovanou aktivací a umlčováním narušené exprese imprintovaných genů. Tento přehled popisuje hlavní epigenomové editory založené na CRISPR a poukazuje na jejich potenciální využití ve výzkumu a terapii vzácných imprintingových onemocnění.
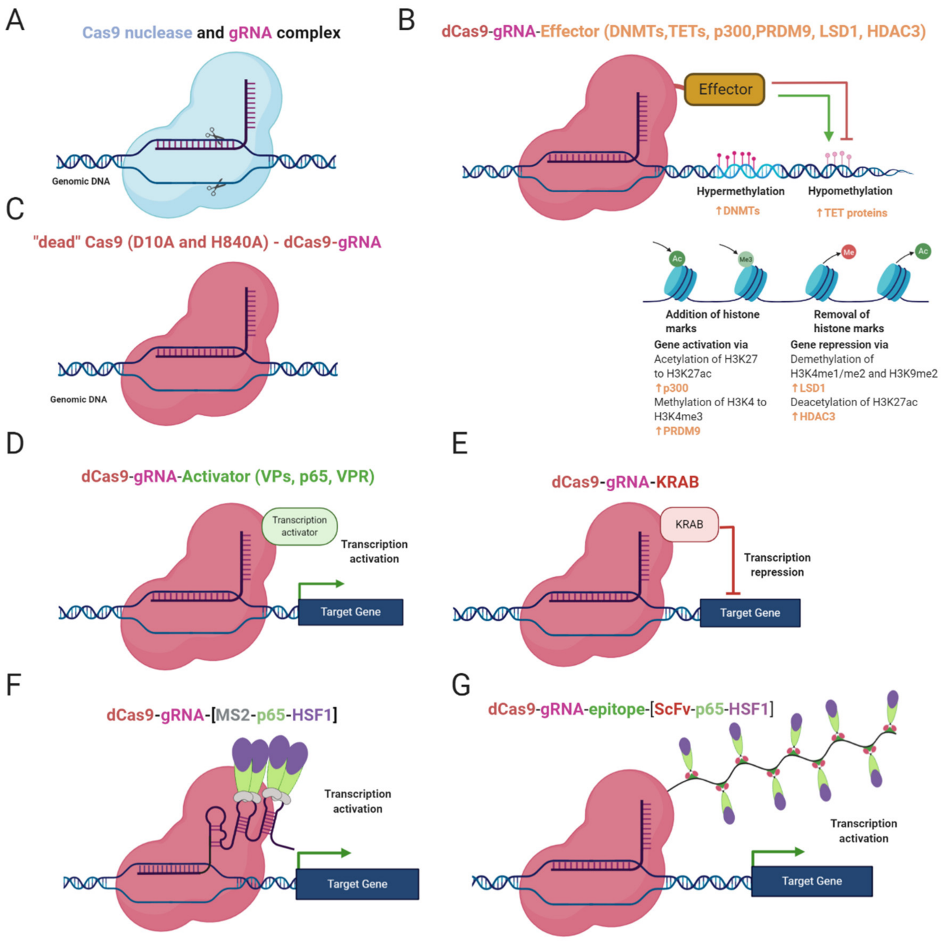
Závěry:
Nový pokrok v oblasti editorů epigenomu CRISPR/Cas9 poskytuje slibné nástroje pro úpravu a případnou léčbu vzácných IN. Mrtvý Cas9 fúzovaný nebo navázaný na „epi-efektorovou“ doménu může modulovat genovou expresi většinou myslitelných způsobů, které jsou schopny zmírnit nebo léčit vzácné ID způsobené aberantní genovou expresí imprintovaných genů. Editory epigenomu založené na systému CRISPR/Cas tak představují nové způsoby aktivace existujících, ale umlčených alel na druhém rodičovském chromozomu nebo způsoby snížení exprese genů, které jsou nesprávně bialelicky exprimovány. Terapeutický potenciál zkoumaných systémů je však omezený, protože je třeba dále vyvíjet účinné doručovací systémy. Je také zapotřebí dalšího zkoumání, aby bylo možné určit kritické terapeutické okno pro každou jednotlivou chorobu. I když je před námi ještě mnoho výzev, systémy CRISPR nepochybně otevřely nové dveře pro léčbu vzácných imprintingových nemocí na základě editace epigenomu, což dříve nebylo možné.
d



